摘要
戈沙妥珠单抗(SG)是靶向TROP2的新型ADC药物,在乳腺癌领域SG已获得国内外批准,用于治疗既往接受过至少两种系统治疗(其中至少一种为针对转移性疾病的治疗)的不可切除局部晚期或转移性三阴性乳腺癌(TNBC)成人患者。 近日,由研究者发起的NeoSTAR研究报告了SG新辅助治疗TNBC的主要结果,目前已全文发表在《肿瘤学年鉴》(Annals of Oncology)杂志上。CCMTV小编特此编译,以飨读者。
研究亮点
1、SG新辅助治疗局部TNBC安全可行;
2、约2/3的患者对SG单药治疗有响应,30%的患者无需额外化疗即可达到病理完全缓解(pCR); 3、更高Ki-67和肿瘤浸润淋巴细胞(TILs)可预测SG的pCR,而TROP2表达则不能预测SG的pCR。 背景
TNBC约占所有乳腺癌的15%~20%,由于缺乏靶点和广泛的异质性,TNBC的治疗选择有限,相比其他乳腺癌亚型,TNBC患者的预后更差。近年来,新辅助治疗的广泛应用改善了TNBC的疗效。新辅助治疗不仅让患者更早开始接受系统治疗,还发现新辅助治疗后达到pCR是改善TNBC患者长期预后的生物标志物。
目前,局部TNBC的最新进展免疫治疗+化疗方面,3期KEYNOTE-522研究显示,对于Ⅱ/Ⅲ期TNBC患者,帕博利珠单抗+新辅助化疗组较安慰剂+化疗组提高13.6%的pCR率,并且pCR的改善转化为长期疗效的改善。然而,多剂帕博利珠单抗-化疗方案显示出明显的毒性,78%的患者发生≥3级不良事件(AE)。TNBC领域迫切需要高效低毒的新辅助治疗方案。
SG是一种靶向TROP2的ADC药物,药物抗体比高达7.6:1。基于1/2期IMMU 132-01研究和3期ASCENT研究结果,SG已获得国内外批准。本次报道SG新辅助治疗局部TNBC的NeoSTAR研究疗效和安全性。
方法
NeoSTAR是一项类似I-SPY的平台临床试验。在第一个队列(A1),局部TNBC(肿瘤大小≥1cm,或淋巴结阳性、肿瘤大小不限)患者接受SG单药新辅助治疗,起始剂量为10mg/kg,21天为一周期(d1、d8静脉输注),共4个周期。4周期后,乳腺和/或腋窝存在残留病灶的患者可选择接受额外新辅助治疗,或根据研究研究者的决定进行手术。术后,患者可根据主治医生的决策接受额外辅助治疗。 主要终点为pCR率(定义为ypT0isN0),次要终点包括客观缓解率(ORR)、安全性、耐受性、无事生存期(EFS)和生活质量。探索性终点包括预测性生物标志物的评估,包括基线Ki-67、TILs和TROP2表达。 图. 研究设计
结果
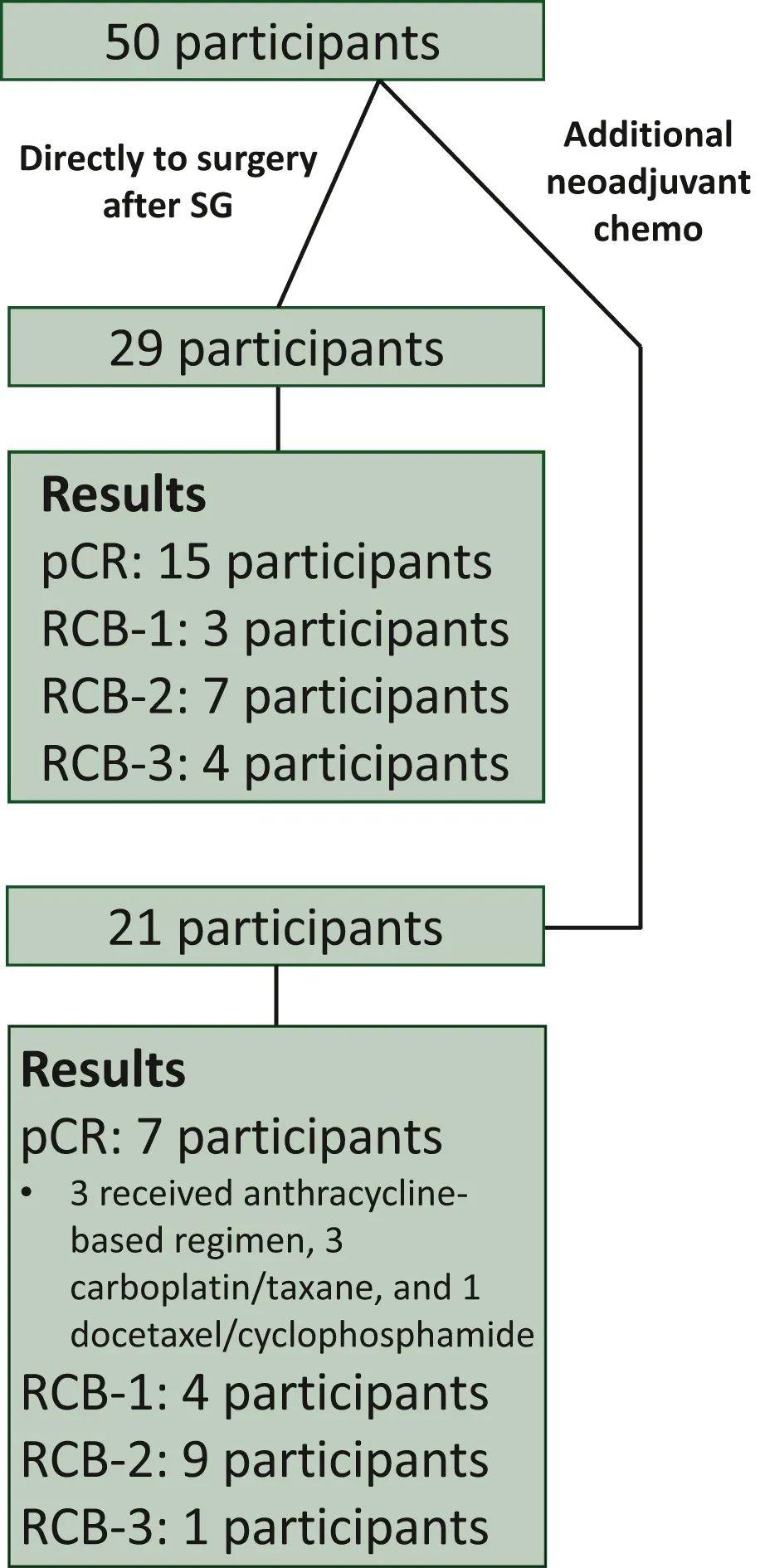
2020年7月14日~2021年8月31日,共入组50例患者,中位年龄48.5岁,大多为临床Ⅱ期疾病(26例,52%),78%的患者淋巴结阴性。98%的患者(49例)完成4周期SG治疗,1例患者因疗效甚微而经研究者酌情决定提前停止治疗。29例患者在SG治疗后直接接受手术,其余患者接受了额外的新辅助治疗。
图. 研究流程图 病理和影像学结果
SG单药新辅助治疗的总体pCR率为30%。Ⅰ期患者的pCR率最高,达50%,而Ⅱ期和Ⅲ期患者的pCR率分别为27%和18%。 在携带BRCA基因致病变异的患者(9例)中,6例达到pCR,pCR率为66.7%。 图. 根据基线临床分期和BRCA突变状态分析的pCR率
SG单药新辅助治疗的总体ORR为64%,Ⅰ期、Ⅱ期和Ⅲ期患者的ORR分别为54%、69%和64%。
无BRCA基因致病变异患者(40例)的ORR为67.5%,其中27例达到(CR)或部分缓解(PR),12例达到疾病稳定(SD),1例疾病进展。
携带BRCA基因致病变异患者(9例)的ORR为55.6%,其中5例达到CR/PR,4例达到SD。
生物标志物结果
基线Ki67、TROP2表达和TILs与pCR vs non-pCR的关系如下图所示。45例患者(90%)伴基线Ki-67、TROP2表达和可评估的TILs。
SG单药新辅助治疗达到pCR的患者的基线Ki67与那些具有残留病灶的患者相比,平均基线Ki67提高16.2%(71.5 vs 55.3,P=0.007)。
pCR患者 vs 残留病灶患者的TROP2表达肿瘤细胞比例方面没有明显差异(P=0.440),H评分也没有明显差异(P=0.626)。
pCR和non-pCR患者的TILS相比,达到pCR者的基线TIL值较non-pCR患者提高24%(55% vs 31%,P=0.002)。
图. 根据生物标志物状态评估的pCR
图. 根据基线生物标志物和BRCA状态分层的瀑布图
长期结果
中位随访18.9个月,所有患者的2年EFS率为95%(下图A)。4周期SG治疗后达到pCR患者的2年EFS率高达100%,SG治疗后存在残留病灶患者的2年EFS率为92%(下图B)。
50例患者中有2例发生EFS事件(2例乳腺癌死亡病例),均发生于有残留病灶组。
图. 整体EFS(A)、4周期SG治疗后达到pCR患者 vs 残留病灶患者的EFS(B)
安全性
最常见的所有级别治疗期间AE为恶心、疲劳、脱发、皮疹、中性粒细胞减少和贫血。所有患者中,98%的患者完成全部4周期SG治疗,6%的患者需要剂量减少。无患者因疾病进展或AE停药。
图. SG治疗期间最常见的AE
讨论&结论
NeoSTAR研究是第一项评估术前SG单药新辅助治疗对局部未经治TNBC患者疗效的临床试验,pCR率为30%,ORR为64%。与更高疾病分期患者相比,Ⅰ期患者的pCR率更高,并且携带BRCA致病变异患者的pCR率也更高。SG新辅助治疗的耐受性普遍良好,AE与SG已知的安全性特征一致。EFS结果尚未成熟但令人鼓舞,中位随访18.9个月后仅发生2起事件。值得注意的是,截至目前所有接受4周期SG治疗的患者均未出现疾病复发。
基线生物标志物数据表明,TROP2的表达不能预测pCR,既往研究也证明了这一点。缺乏关联性的可能原因有分析因素(检测类型、评分方法)或统计因素(样本量小),也可能确实与生物学无关。值得注意的是,在SG治疗转移性TNBC的ASCENT研究中,TROP2表达也与疗效之间没有线性关系。此外,与化疗观察到的情况类似,更高的Ki-67和TIL可预测SG的疗效。
总体而言,NeoSTAR研究证明了单药SG新辅助治疗对局部TNBC的疗效,以及根据初始疗效在疗效指导下升阶梯/降阶梯的可行性。TNBC患者的疗效改善离不开持续的新型治疗探索。目前正在对局部TNBC(队列A2)、HR+乳腺癌(队列B)和HER2-炎性乳腺癌(队列C)患者进行SG+免疫新辅助治疗的探索,未来可期!
参考文献
REFERENCES
Spring LM, Tolaney SM, Fell G, et al. Response-guided neoadjuvant sacituzumab govitecan for localized triple-negative breast cancer: results from the NeoSTAR trial. Ann Oncol. 2023 Dec 12:S0923-7534(23)05107-4.
编辑|梅婕
审核|叶静 责编|赵德云
— END — 汇集最新最全的肿瘤资讯
欢迎关注CCMTV临床频道·肿瘤之音!
点击下方“阅读原文” 访问更多CCMTV肿瘤科频道精彩内容
二维码
关注CCMTV

CCMTV APP下载

关注CCMTV云管家