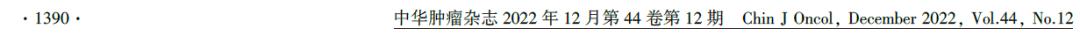吴凡, 陈木兰, 黄伟炜, 等. 人表皮生长因子受体2阳性曲妥珠单抗原发耐药晚期乳腺癌长期缓解1例[J]. 中华肿瘤杂志, 2022, 44(12):1390-1392. DOI:10.3760/cma.j.cn112152-20220620-00437.
患者女,42岁,2018年2月因发现右乳肿物4个月余就诊当地医院,查体示右乳内下、乳头下方肿物4.0 cm×4.0 cm,质硬,固定,右腋窝淋巴结肿大2.0 cm×2.0 cm。2018年3月4日行右乳腺癌改良根治术,术后病理示右乳浸润性乳腺癌,组织学分级Ⅱ级,伴导管原位癌(约占5%);乳头、乳腺表面皮肤未见癌累及;腋窝淋巴结(13/28)见癌转移。免疫组化结果示雌激素受体(estrogen receptor, ER)15%+,孕激素受体(progesterone receptor, PR)5%+,人表皮生长因子受体2(human epidermal growth factor receptor 2, HER-2)3+,Ki-67 30%~40%阳性。荧光原位杂交示HER-2基因扩增。2018年4月至2019年6月行表柔比星+环磷酰胺序贯紫杉醇+曲妥珠单抗8个周期辅助化疗及曲妥珠单抗靶向治疗满1年,治疗期间出现2度白细胞下降,粒细胞集落刺激因子(granulocyte colony-stimulating factor G-CSF)升白治疗后恢复正常。患者因个人原因未行辅助放疗及辅助内分泌治疗。
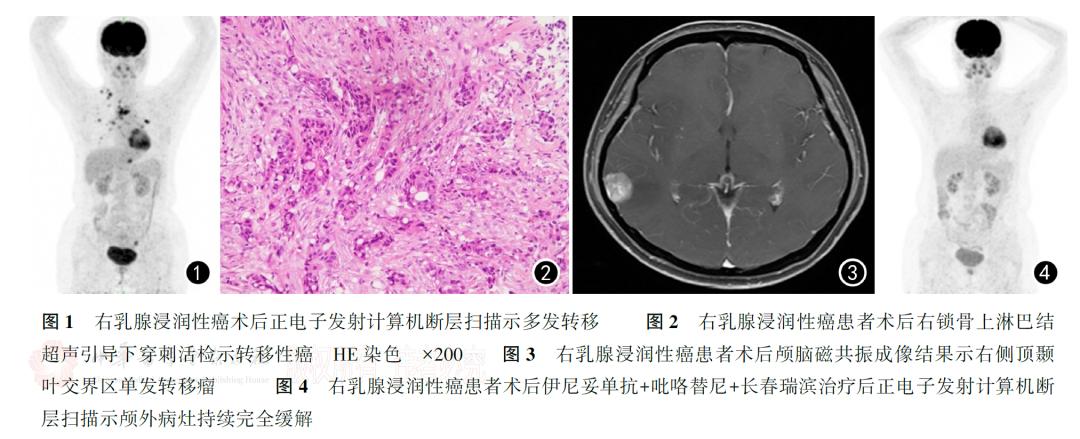
2020年4月出现干咳,2020年5月入我院。5月10日正电子发射计算机断层扫描(positron emission tomography/computed tomography, PET-CT)示右锁骨区、纵隔、肺门淋巴结转移,双肺转移,左第6后肋转移,肝S3转移(图1)。行超声引导下右锁骨上淋巴结穿刺,病理示转移性癌;免疫组化结果:ER阳性(50%,强弱不等),PR阳性(40%,强弱不等),HER2 3+,Ki-67阳性(约40%),AR(+,90%,中等-强),GATA3(+);免疫组化结果见图2,结合病史及免疫组化结果符合乳腺癌转移,诊断为右乳浸润性癌(pT2N3M0 ⅢC期)术后治疗后淋巴结、肺、骨、肝转移。患者属于曲妥珠单抗治疗失败(原发耐药),建议使用抗体偶联药物(antibody-drug conjugates, ADC)T-DM1,患者因经济因素拒绝。对于激素受体阳性HER-2阳性晚期乳腺癌,各项指南仍推荐靶向联合化疗作为优选,仅在无法耐受化疗或化疗联合靶向后维持治疗时采用靶向联合内分泌。2020年6月开始伊尼妥单抗(8 mg/kg首次,6 mg/kg后续,第1天静脉滴注,每3周1次)+吡咯替尼(400 mg,口服,1次/d)+长春瑞滨(25 mg/m2,第1天、第8天静脉滴注,每3周1次)治疗,共8个周期。治疗过程患者出现2度白细胞下降,G-CSF升白治疗后好转,1级腹泻,思密达治疗后好转。2个周期后复查PET-CT疗效评估完全缓解(complete response, CR),8个周期评估持续CR。后续患者不愿继续化疗,查E2处于绝经期水平,2021年2月开始予伊尼妥单抗(6 mg/kg,静滴第1天,每3周1次)+吡咯替尼(400 mg口服1次/d)+依西美坦(25 mg口服1次/d)维持治疗,治疗过程出现1级腹泻,思密达治疗后好转。2021年11月患者诉头晕,头部磁共振成像(magnetic resonance imaging, MRI)示右侧顶颞叶交界区单发转移瘤(图3);颈胸腹CT示颅外病灶持续CR。2021年12月行脑部放疗(5000 cGy分10次完成),继续伊尼妥单抗+吡咯替尼+依西美坦全身治疗至2022年8月。2022年8月8复查颅脑MRI提示颅内病灶部分缓解,PET-CT示颅外病灶持续CR(图4)。
讨 论
乳腺癌居我国女性恶性肿瘤发病首位,20%~25%的浸润性乳腺癌HER-2阳性,是乳腺癌预后不良的独立危险因素。抗HER-2靶向治疗已在临床上广泛应用,研究已证实曲妥珠单抗为HER-2阳性乳腺癌术后标准靶向治疗。但由于耐药的出现使得患者难以获得长期获益。约30%的患者出现曲妥珠单抗原发耐药,40%的患者会出现获得性耐药,使用辅助曲妥珠单抗的患者2年复发率为8.0%~11.5%,4年复发率为14%~21%。曲妥珠单抗原发耐药(或称曲妥珠单抗治疗失败)是指转移性乳腺癌经曲妥珠单抗治疗8~12周内出现疾病进展,或第1次影像学疗效评价即出现疾病进展,早期乳腺癌术后辅助曲妥珠单抗治疗过程中出现复发转移,或曲妥珠单抗治疗结束后12个月内出现复发转移。
曲妥珠单抗原发耐药治疗难度大,可选的后续靶向药物较少。目前国际指南推荐ADC类药物(DS-8201, T-DM1)已取代酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)+卡培他滨成为标准的二线治疗药物,2022版美国国立综合癌症网络指南已将DS-8201作为二线治疗的首选方案,但昂贵的价格限制了其临床广泛应用。国内指南还推荐吡咯替尼+卡培他滨作为原发性曲妥珠单抗耐药的优选方案,但吡咯替尼和卡培他滨均有较明显的3级腹泻发生率,患者使用依从性较差,且中位无进展生存时间(progression free survival, PFS)也仅1年左右。因此对于曲妥珠单抗原发耐药患者的大量临床需求仍未被满足。
结合我国国情,我们希望在吡咯替尼联合化疗的基础上进一步提高HER-2原发耐药患者的生存获益。既往研究显示,HER-2单克隆抗体联合小分子TKI是曲妥珠单抗治疗失败后的一种新型治疗策略,EGF104900、HER2CLIMB、CALGB40601、PHEDRA等研究均显示,在存在肿瘤负荷的情况下HER-2单克隆抗体联合小分子TKI显示出优于单一抗HER-2靶向治疗的效果。在此基础上,我们用Fc段改构的曲妥珠单抗(伊尼妥单抗)代替曲妥珠单抗以期进一步提高曲妥珠单抗原发耐药患者的获益。伊尼妥单抗是中国自主研发的Fc段改构HER-2重组人源化单克隆抗体,其抗体依赖细胞介导的细胞毒性是曲妥珠单抗的1.1倍。HOPES研究已证实伊尼妥单抗在晚期HER-2阳性乳腺癌中的有效性和安全性。既往SOPHIA研究显示,Fc段改构的Margetuximab可改善HER-2阳性晚期乳腺癌的PFS。因此,我们探索性应用伊尼妥单抗+吡咯替尼+长春瑞滨在曲妥珠单抗原发耐药(无法使用ADC类药物)患者的临床疗效和安全性,并取得了良好的疗效,PFS长达2年,并且安全性良好。伊尼妥单抗与吡咯替尼联合应用起到HER-2受体细胞内外双重阻断、里应外合的抗肿瘤效应。中国双靶(伊尼妥单抗+吡咯替尼)是曲妥珠单抗原发耐药后续靶向治疗中新的有益尝试,值得进一步探索。
CCMTV肿瘤频道视频号已上线!
带您洞察肿瘤前沿资讯 精彩不断,敬请关注!
免费阅读原文
二维码
关注CCMTV

CCMTV APP下载

关注CCMTV云管家