摘要
一年一度的肺癌领域学术盛会世界肺癌大会(WCLC)即将于2023年9月9日~12日召开。日前,除Plenary Session之外的摘要已公布,CCMTV小编带您一文速览ADC药物Oral专场4项最新研究进展,包括HER3 ADC药物Patritumab Deruxtecan(HER3-DXd)、Trop2 ADC药物戈沙妥珠单抗(SG)和Datopotamab Deruxtecan(Dato-DXd),以及B7-H3 ADC药物Ifinatamab Deruxtecan(I-DXd;DS-7300)。 1、HERTHENA-Lung01研究:Patritumab Deruxtecan(HER3-DXd)用于EGFR-TKI和含铂化疗治疗后的EGFR突变NSCLC(OA05.03)
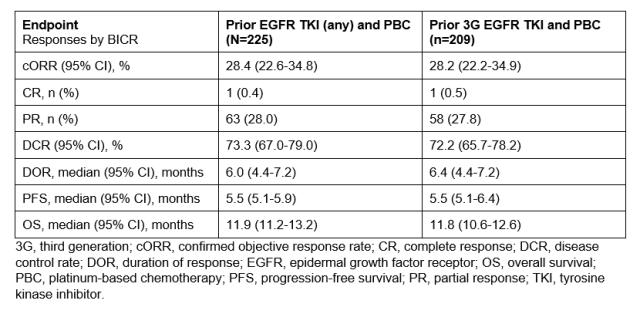
2期、开放标签HERTHENA-Lung01研究纳入既往EGFR-TKI和含铂化疗经治的晚期EGFR突变非小细胞肺癌(NSCLC)患者,接受HER3-DXd 5.6mg/kg IV Q3W或递增方案(3.2~4.8~6.4mg/kg)。基于1期数据的获益-风险评估,递增组的入组提前结束;5.6mg/kg组的入组已完成。主要终点为盲态独立中央评审委员会(BICR)评估的确认客观缓解率(cORR)。 5.6mg/kg组中,225例患者接受HER3-DXd治疗。截至2022年11月21日,中位研究持续时间13.1个月,中位治疗持续时间5.5个月。cORR为28.4%,中位缓解持续时间(DOR)为6.0个月,中位无进展生存期(PFS)为5.5个月,中位总生存期(OS)为11.9个月。在广泛经治的HER3表达和不同EGFR-TKI耐药机制的患者中观察到临床活性。在基线未经放疗的脑转移患者中(n=30),中枢神经系统(CNS)cORR为36.7%,10/30例患者达到完全缓解。
不良事件(AE)整体可控可耐受,与既往的观察结果一致。10例患者(4.4%)的停药以及4例患者(1.8%)的死亡与药物相关AE有关。≥3级药物相关AE发生率为45.3%。经独立判定,药物相关间质性肺病发生率为5.3%(9例1/2级,2例3级,1例5级)。
结论
在这类存在明显未满足需求和有限治疗选择的患者中,HER3-DXd表现出具有临床意义的疗效,此外,本研究还首次报道了HER3-DXd在CNS中的疗效。安全性整体可控。HER3-DXd是既往经治的EGFR突变NSCLC患者极具潜力的治疗选择。针对EGFR-TKI治疗进展后的EGFR突变NSCLC,3期HERTHENA-Lung02研究(NCT05338970)目前正在进行中。 2、EVOKE-02研究:戈沙妥珠单抗(SG)+帕博利珠单抗一线治疗转移性NSCLC的初步结果(OA05.04)
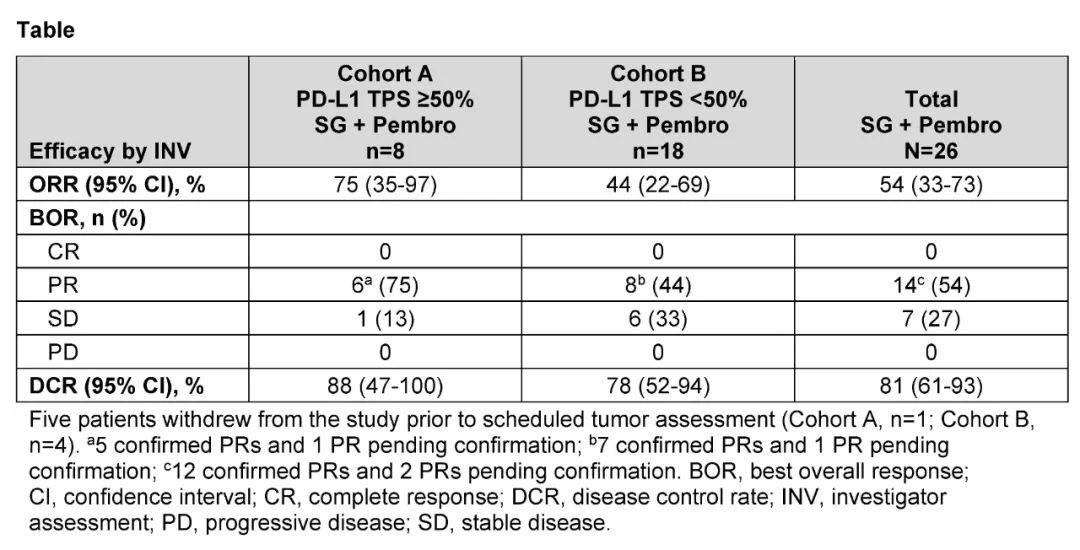
全球、开放标签、多队列、2期EVOKE-02研究(NCT05186974)旨在评估Trop2 ADC药物SG+帕博利珠单抗±铂类化疗一线治疗mNSCLC,本次报道队列A和B中SG+帕博利珠单抗治疗的初步结果。PD-L1 TPS≥50%(队列A)和PD-L1 TPS<50%(队列B)患者,接受SG 10mg/kg D1和8+帕博利珠单抗200mg D1,21天为1周期。研究终点包括ORR、PFS、DOR、疾病控制率(DCR)、OS和安全性。 截至2023年1月13日,队列A 16例和队列B 28例共44例患者接受SG+帕博利珠单抗治疗。疗效可评估患者(队列A 8例和队列B 18例)中,队列A的ORR为75%,队列B的ORR为44%。 安全性评估患者(n=44)中,3/4级TEAE发生率为52%。最常见的任意级别TEAE为腹泻(50%)、贫血(41%)、乏力(36%)和中性粒细胞减少症(32%)。因TEAE导致SG停药率为7%。3例患者(7%)因TEAE死亡,仅1例(2%)被认为与研究治疗相关。
结论
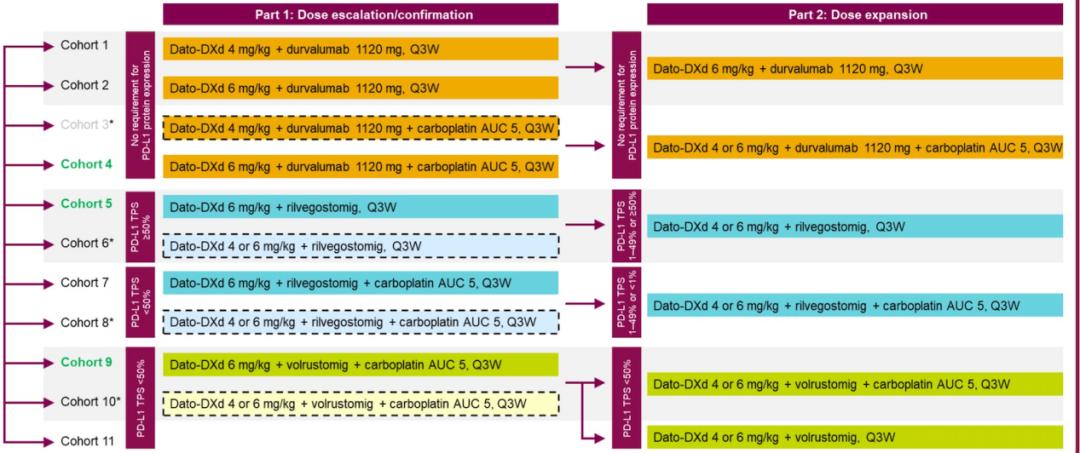
在队列A和B中,SG+帕博利珠单抗治疗初治的mNSCLC患者表现出令人鼓舞的早期疗效和可控的安全性,与各药物已知的安全性一致。 3、1b期TROPION-Lung04研究初步结果:Datopotamab Deruxtecan(Dato-DXd)+度伐利尤单抗±卡铂治疗晚期/转移性NSCLC(OA05.06) 针对晚期/mNSCLC的1b期、多中心、开放标签、剂量递增/确认和扩展的TROPION-Lung04研究(NCT04612751)中期分析首次报道队列1~4的数据。队列1的患者和队列2中的1例患者接受过≥1线含铂化疗和抗PD-1/L1治疗。随后的患者为初治或接受过≤1线系统性化疗,没有ICI。患者接受Trop2 ADC药物Dato-DXd(队列1/3为4mg/kg,队列2/4为6mg/kg)+度伐利尤单抗(所有队列1120mg)+至多4周期卡铂(队列3/4 AUC=5),Q3W直至疾病进展或不可耐受的毒性。在第一部分(剂量递增/确认)试验中,队列1-4队列采用3~6例患者的mTPI-2设计。基于观察到的剂量限制毒性(DLT),第2部分(剂量扩展)被开放(队列3是一个必要的降级队列)。主要终点为安全性/耐受性。次要终点包括研究者评估的ORR和DCR。
截至2023年3月6日,队列1(n=5)、队列2(n=19)和队列4(n=14)的38例患者疗效可评估。队列4的2例患者报告DLT,1例3级发热性中性粒细胞减少症;1例3级黄斑丘疹性皮疹和口腔炎导致第2周期延迟2周以上。随后队列2(双药)和队列4(三药)剂量扩展也未观察到进一步的DLT。
队列2/4中,73.7%/92.9%的患者为初治晚期/mNSCLC,PD-L1表达<1%、1%~49%和≥50%的患者比例分别为31.6%/42.9%、31.6%/21.4%和36.8%/35.7%,中位治疗周期数为8.0/8.5,31.6%/50.0%的患者仍在治疗中。
队列2一线治疗的患者中,ORR为50.0%,DCR为92.9%;队列4一线治疗的患者中,ORR为76.9%,DCR为92.3%。疗效可见于所有PD-L1表达水平的患者,三药疗效整体上优于双药。
队列2最常见的TEAE(所有级别/≥3级)为便秘(57.9%/0)、口腔炎(52.6%/10.5%)、脱发(52.6%/0)和恶心(42.1%/0);队列4中为口腔炎(64.3%/7.1%)、脱发(57.1%/0)、恶心(57.1%/0)、贫血(50.0%/35.7%)。队列2/4中,因TEAE导致停药和Dato-DXd减量发生率分别为21.1%/21.4%和15.8%/35.7%。无治疗相关死亡事件。
结论
Dato-DXd+度伐利尤单抗±卡铂治疗晚期/mNSCLC安全性可控,抗肿瘤活性令人鼓舞。 4、Ifinatamab Deruxtecan(I-DXd;DS-7300)治疗复发性SCLC:一项1/2期研究亚组分析(OA05.05)
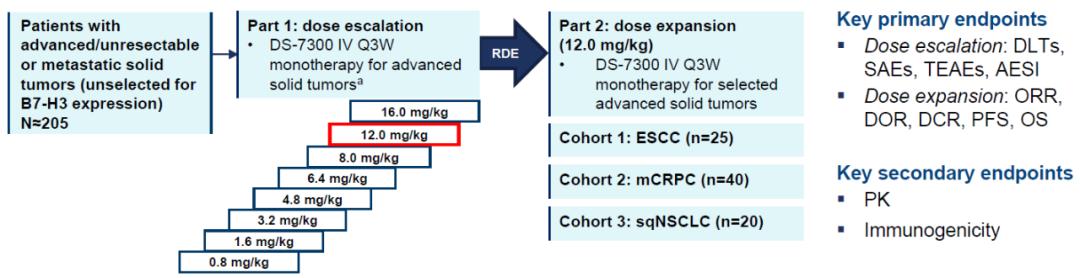
I-DXd是一种靶向B7-H3的新型ADC药物。2022年ESMO大会上报道了I-DXd治疗多线经治晚期实体瘤患者的1/2期研究结果(相关阅读:2022 ESMO | ADC新秀!B7-H3 ADC药物DS-7300治疗SCLC,ORR高达53%,并对多种实体瘤有效)。本次报道中位随访11.7个月后,I-DXd 4.8~16.0mg/kg治疗第一部分中SCLC亚组的ORR、PFS、OS,以及基于B7-H3表达的疗效分析。 截至2023年1月31日,21例SCLC患者疗效和安全性可评估。目前2例患者仍在治疗。患者既往接受中位2线治疗,大多为含铂化疗和免疫治疗经治。安全性与既往报道一致。ORR为52%,其中1例患者达到完全缓解,10例部分缓解。中位DOR为5.9个月,中位PFS为5.8个月,中位OS为9.9个月。
截至2022年6月30日,16例患者的B7-H3可评估,B7-H3表达水平均为中等至高表达。最佳缓解或肿瘤缩小与B7-H3阳性或高表达之间没有关联,未来还需更大样本量的研究进行验证。
结论
I-DXd为多线经治的SCLC患者带来持久稳健的疗效,安全性可控可耐受。近期一项专门针对广泛期SCLC二或三线治疗的2期研究(NCT05280470)正在进行中。
参考文献
REFERENCES
1. H.A. Yu, et al. Patritumab Deruxtecan (HER3-DXd) in EGFR-Mutated NSCLC Following EGFRTKI and Platinum-Based Chemotherapy: HERTHENA-Lung01. 2023 WCLC Abs OA05.03.
2. B.C. Cho, et al. Sacituzumab Govitecan + Pembrolizumab in 1L Metastatic Non-Small Cell Lung Cancer: Preliminary Results of the EVOKE-02 Study. 2023 WCLC Abs OA05.04.
3. K.P. Papadopoulos, et al. Datopotamab Deruxtecan (Dato-DXd) + Durvalumab ± Carboplatin in Advanced/mNSCLC: Initial Results from Phase 1b TROPION-Lung04. 2023 WCLC Abs OA05.06.
4. M. Johnson, et al. Ifinatamab Deruxtecan (I-DXd; DS-7300) in Patients with Refractory SCLC: A Subgroup Analysis of a Phase 1/2 Study. 2023 WCLC Abs OA05.05. 编辑|梅婕 审核|叶静 责编|赵德云 — END — 汇集最新最全的肿瘤资讯
欢迎关注CCMTV临床频道·肿瘤之音!
点击下方“阅读原文” 访问更多CCMTV肿瘤科频道精彩内容
二维码
关注CCMTV

CCMTV APP下载

关注CCMTV云管家