摘要
一年一度的肺癌领域学术盛会世界肺癌大会(WCLC)即将于2023年9月9日~12日召开。日前,除Plenary Session之外的摘要已公布,CCMTV小编带您一文速览晚期非小细胞肺癌(NSCLC)免疫治疗Oral专场——斯鲁利单抗ASTRUM-004研究、阿替利珠单抗IMpower151研究、度伐利尤单抗ILLUMINATE研究,以及STK11/LKB1缺失与免疫治疗疗效关系的4项最新研究进展。 值得骄傲的是,4项研究中的3项都是由中国专家带来的汇报,分别为同济大学附属上海市肺科医院周彩存教授(ASTRUM-004研究、IMpower151研究)和中山大学肿瘤防治中心张力教授、洪少东教授团队的李岸霖教授(STK11/LKB1缺失与免疫治疗疗效关系)。 1、3期ASTRUM-004研究:斯鲁利单抗+化疗一线治疗鳞状NSCLC(OA09.05)
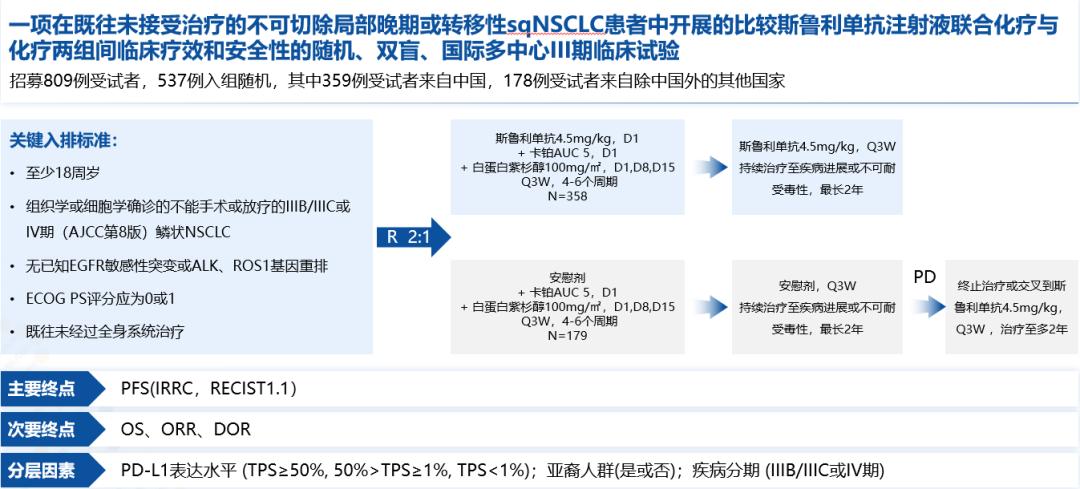
随机、双盲、国际多中心3期研究纳入初治的ⅢB/ⅢC或Ⅳ期NSCLC患者,按2:1随机接受新型PD-1抑制剂斯鲁利单抗4.5mg/kg或安慰剂(至多35周期)+化疗(卡铂和白蛋白紫杉醇,4~6周期),3周为1周期。根据PD-L1表达水平(TPS≥50% vs 1%≤TPS<50% vs TPS<1%)、人种(亚裔 vs 非亚裔)和疾病分期(ⅢB/ⅢC期 vs Ⅳ期)分层分析。主要终点为独立放射审查委员会(IRRC)评估的无进展生存期(PFS),次要终点包括其他疗效指标、安全性和生物标志物探索。
本次报道预设的总生存期(OS)最终分析,以及PFS和安全性更新分析。截至2023年1月31日,537例患者随机分配至斯鲁利单抗-化疗组(n=358)或安慰剂-化疗组(n=179)。中位随访31.1个月,斯鲁利单抗-化疗组的PFS持续获益,两组分别为8.3个月 vs 5.7个月(HR=0.55),各预设亚组均可从斯鲁利单抗-化疗组获得PFS获益。斯鲁利单抗-化疗组的OS较安慰剂-化疗组显著延长,中位OS分别为22.7个月 vs 18.2个月(HR=0.73,P=0.010)。 安全性方面,两组中与斯鲁利单抗或安慰剂相关的≥3级不良事件(AE)发生率为35.5%和31.8%,最常见的为中性粒细胞计数下降(14.8% vs 14.5%)、贫血(12.0% vs 10.6%)和白细胞计数下降(10.1% vs 11.2%)。两组的免疫相关不良事件(irAE)发生率分别为29.6%和17.3%,最常见的为甲状腺功能减退症(6.4% vs 0.6%)、皮疹(5.0% vs 1.1%)和免疫介导的肺部疾病(4.2% vs 0.6%)。 结论
与安慰剂+化疗相比,斯鲁利单抗+化疗显著改善既往经治的局部晚期或转移性NSCLC患者,安全性可控。斯鲁利单抗+化疗有望成为这类患者的治疗新选择。 2、3期IMpower151研究:阿替利珠单抗+贝伐珠单抗+化疗一线治疗转移性非鳞NSCLC(OA09.06)
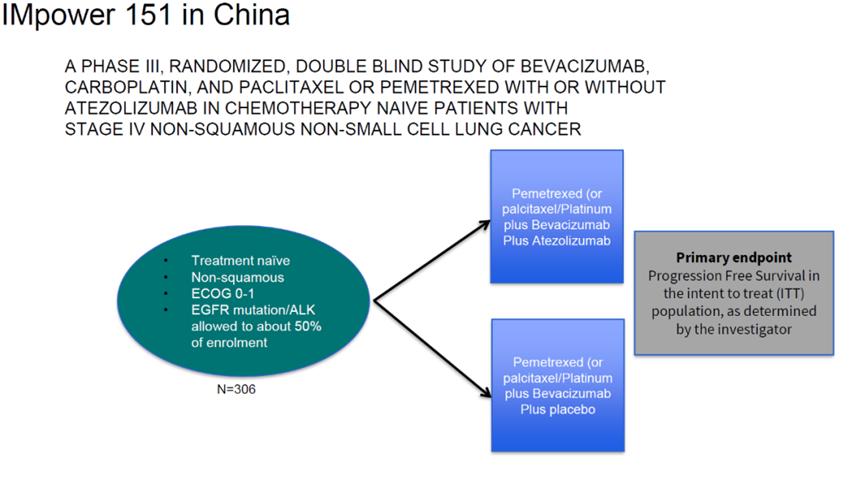
基于IMpower150研究结果,PD-L1抑制剂阿替利珠单抗+贝伐珠单抗+化疗已获批一线治疗EGFR/ALK阴性转移性非鳞NSCLC。为了解决患者基因突变情况(如EGFR突变发病率)和临床实践(如应用培美曲塞)的区域差异问题,在中国开展了3期IMpower151(NCT04194203)研究。
纳入未经化疗治疗的转移性非鳞NSCLC患者,1:1接受阿替利珠单抗/安慰剂(1200mg)+贝伐珠单抗(15mg/kg)+卡铂(AUC=6)+紫杉醇(175mg/m2)或培美曲塞(500mg/m2)IV Q3W,4周期治疗,随后阿替利珠单抗/安慰剂维持治疗直至不可耐受的毒性或无临床获益,以及贝伐珠单抗和培美曲塞(若诱导治疗期间应用)直至进展。分层因素为EGFR/ALK基因类型(突变 vs 野生型,野生型上限为50%)和PD-L1表达(SP263检测肿瘤细胞<50% vs ≥50%)。主要终点为意向治疗人群(ITT)研究者(INV)评估的的PFS,次要终点包括EGFR/ALK+人群的INV-PFS、PD-L1亚组的INV-PFS、独立审查(IRF)评估的PFS、OS、客观缓解率(ORR)和缓解持续时间(DOR)。
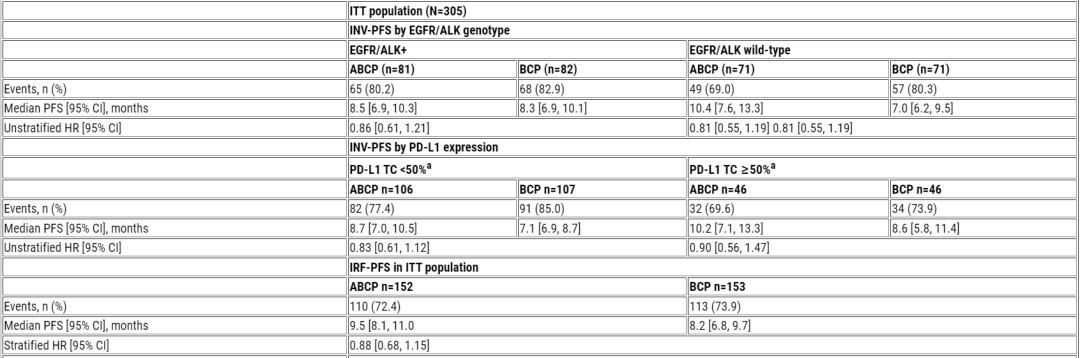
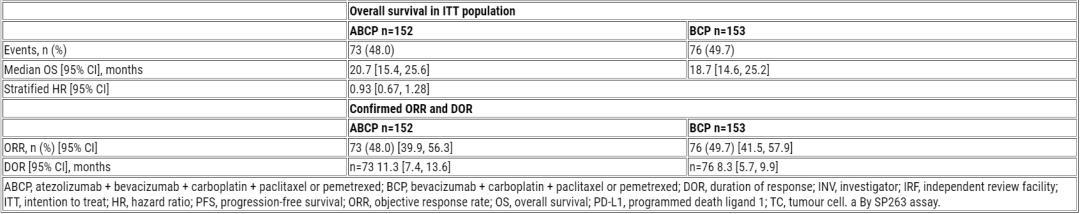
截至2023年2月2日,中位随访14个月。305例患者(ITT人群)中,297例(97.4%)应用培美曲塞。研究未达主要终点,ABCP vs BCP的中位INV-PFS为9.5个月 vs 7.1个月(HR=0.84,P=0.1838)。INV-PFS与IRF-PFS一致。EGFR/ALK+亚组中,两组的PFS相近,但在EGFR/ALK野生型亚组中显示出数值上的差异(10.4个月 vs 7.0个月)。PD-L1与PFS无关联。
安全性方面,ABCP组与BCP组的全因3/4级AE发生率为66.4% vs 61.4%,导致任何治疗停药率为23.0% vs 15.0%,5级治疗相关AE发生率为5.9%和6.5%。
结论
IMpower151研究未达到INV-PFS主要终点,ABCP vs BCP观察到PFS和OS数值上的改善。ABCP整体耐受性良好,未观察到新发安全性信号。 3、ILLUMINATE研究:度伐利尤单抗联合Tremelimumab和化疗治疗EGFR抑制剂治疗进展的EGFR突变NSCLC的疗效和安全性(OA09.04) 这项国际、非比较、双队列研究纳入来自10个澳大利亚中心和6个中国台湾中心的患者,队列1纳入组织和血液EGFR T790M阴性、一线奥希替尼或后续单线1/2代TKI进展的患者,队列2纳入组织和/或血液EGFR T790M阳性、≥1线TKI包括奥希替尼治疗进展的患者。患者接受4周期度伐利尤单抗1500mg+Tremelimumab 75mg+铂类-培美曲塞化疗Q3W,随后度伐利尤单抗1500mg+培美曲塞500mg/m2维持治疗Q4W直至疾病进展或不可耐受的毒性。主要终点为ORR,次要终点包括DCR、PFS、12个月PFS率和AE。 2019年4月~2022年11月,纳入100例患者,2个队列各50例。1例不合格的参与者被排除在分析之外。绝大部分患者为亚裔(77%)和非吸烟者(73%),19del和21L858R突变分别为57%和42%。 中位随访22个月,队列1的ORR为31%,DCR为88%,中位PFS为7.0个月,12个月PFS率为35%。PD-L1<50%的患者(n=9)的PFS优于PD-L1≥50%的患者(n=20),中位PFS为9.8个月 vs 4.6个月。 队列2的ORR为21%,DCR为75%,中位PFS为4.9个月,12个月PFS率为13%。 每个队列中,19del和21L858R患者的PFS没有显著差异。 安全性方面,没有发生5级irAE,3~4级irAE发生率为17%,因irAE导致的停药率为6%。两队列间的3~4级irAE发生率无显著差异(10% vs 18%,P=0.40)。 结论
度伐利尤单抗联合Tremelimumab和化疗治疗EGFR-TKI治疗进展的EGFR突变NSCLC,尤其是EGFR T790M阴性患者,抗肿瘤疗效令人鼓舞,安全性与化免方案治疗晚期肺癌的已知AE一致。 4、STK11/LKB1缺失而非突变降低NSCLC的免疫治疗效果:3项随机试验结果(OA09.03)
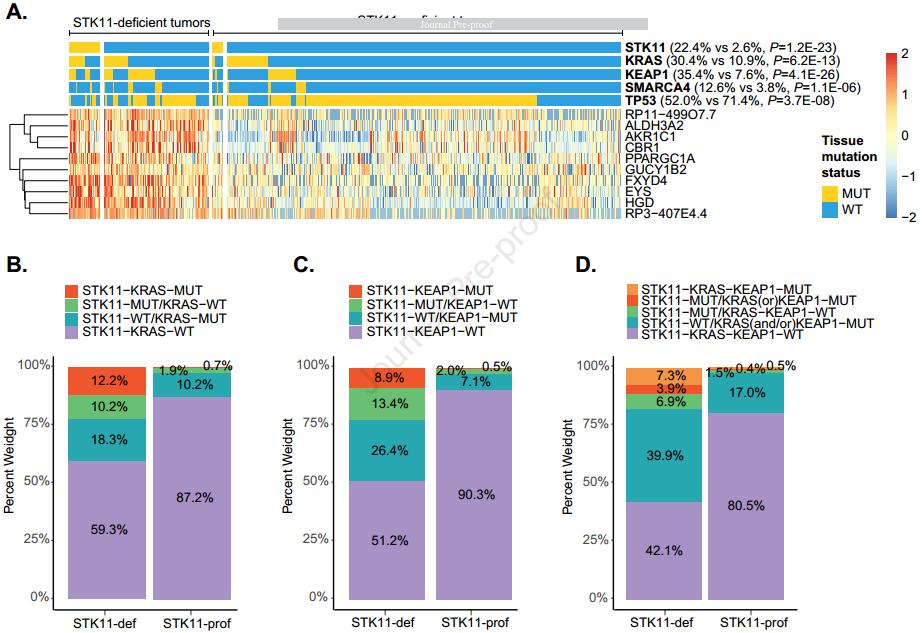
利用选定的功能性STK11突变事件和LKB1蛋白数据,建立了一个基于10个基因转录组学的STK11缺失分类工具。肿瘤分为STK11缺失组或STK11-proficient组。STK11表型与生存率、分子特征的相关性在包括1062例NSCLC患者的3项独立的PD-(L)1随机对照试验中进行了评估,分别为信迪利单抗+化疗 vs 化疗的NCT03607539、阿替利珠单 vs 化疗的NCT02008227和NCT01903993,以及TCGA队列。
组织STK11突变不影响免疫检查点阻断剂(ICB)的疗效。然而在3项ICB研究中,PD-(L)1 vs 化疗的OS获益在STK11缺失肿瘤中消失,HR分别为1.07、0.97和1.61,而OS获益仍可见于STK11-proficient肿瘤,HR分别为0.59、0.81和0.66。PFS方面也观察到相似结果。
评估STK11突变不能检测出45%~70%的STK11缺失病例。
在按表型和突变状态进行不同分类的肿瘤中,STK11野生型/缺失型肿瘤对PD-(L)1抑制剂的疗效较STK11突变/proficient肿瘤显著更差。
STK11缺失的有害影响与STK11/KRAS/KEAP1状态或PD-L1表达无关。
虽然在既往的试验环境中,STING通路的抑制是STK11失活的公认标志,但研究证明STK11缺失表型而不是突变可以有力地反映STING和I型干扰素信号的失活。
最后,在STK11缺失型肿瘤中,高CD8+T细胞不仅不能改善ICB的疗效,甚至负面预测ICB的疗效。这表明STK11缺失与CD8+T细胞功能障碍之间存在关联,而这种关联可能无法通过抑制PD-(L)1来逆转。
结论
与仅考虑STK11突变相比,STK11表型分类工具作为STK11/LKB1失活更广泛的衡量标准,可以更好地区分不太可能从PD-(L)1抑制剂中获益的患者,并启示未来的临床试验设计。对于STING活性降低和ICB不可逆T细胞功能障碍的STK11缺失型NSCLC,亟需采用新的免疫调节策略来改善预后。
参考文献
REFERENCES
1. C. Zhou, et al. A Phase 3 Study of Serplulimab Plus Chemotherapy as First-Line Treatment for Squamous Non-small-Cell Lung Cancer (ASTRUM-004). 2023 WCLC Abs OA09.05. 2. C. Zhou, et al. IMpower151: Phase III Study of Atezolizumab + Bevacizumab + Chemotherapy in 1L Metastatic Nonsquamous NSCLC. 2023 WCLC Abs OA09.06. 3. C. Lee, et al. ILLUMINATE: Efficacy and Safety of Durvalumab-Tremelimumab and Chemotherapy in EGFR Mutant NSCLC Following Progression on EGFR Inhibitors. 2023 WCLC Abs OA09.04. 4. A. Li, et al. STK11/LKB1 Deficient Phenotype Rather Than Mutation Diminishes Immunotherapy Efficacy in NSCLC: Results From Three Randomized Trials. 2023 WCLC Abs OA09.03. 编辑|梅婕 审核|叶静 责编|赵德云 — END — 汇集最新最全的肿瘤资讯
欢迎关注CCMTV临床频道·肿瘤之音!
点击下方“阅读原文” 访问更多CCMTV肿瘤科频道精彩内容
二维码
关注CCMTV

CCMTV APP下载

关注CCMTV云管家