摘要
2023年欧洲肺癌大会(ELCC)即将于3月29日~4月1日在丹麦哥本哈根与线上同步召开,届时全球肺癌领域专家齐聚一堂,共同探讨最新前沿进展。日前,大会日程和摘要题目已公布,CCMTV小编特别就Proffered Paper专场(靶向治疗4项、免疫治疗3项、化疗1项)的研究看点进行整理。
靶向治疗领域:奥希替尼相关治疗、罕见突变(EGFR 20插入突变和KRAS G12C突变)的治疗仍是最大热点;
免疫治疗领域:早期NSCLC CheckMate 816研究热度不减,PD-1+化疗、PD-L1+多靶点TKI,晚期NSCLC免疫联合治疗探索方兴未艾;
化疗领域:亦是唯一入选的SCLC研究抱憾折戟。
1O - Osimertinib versus gefitinib followed by osimertinib in patients with EGFR mutant non-small cell lung cancer (NSCLC): EORTC Lung Cancer Group 1613 APPLE trial
EORTC肺癌组1613 APPLE研究:奥希替尼 vs 吉非替尼序贯奥希替尼治疗EGFR突变非小细胞肺癌(NSCLC)
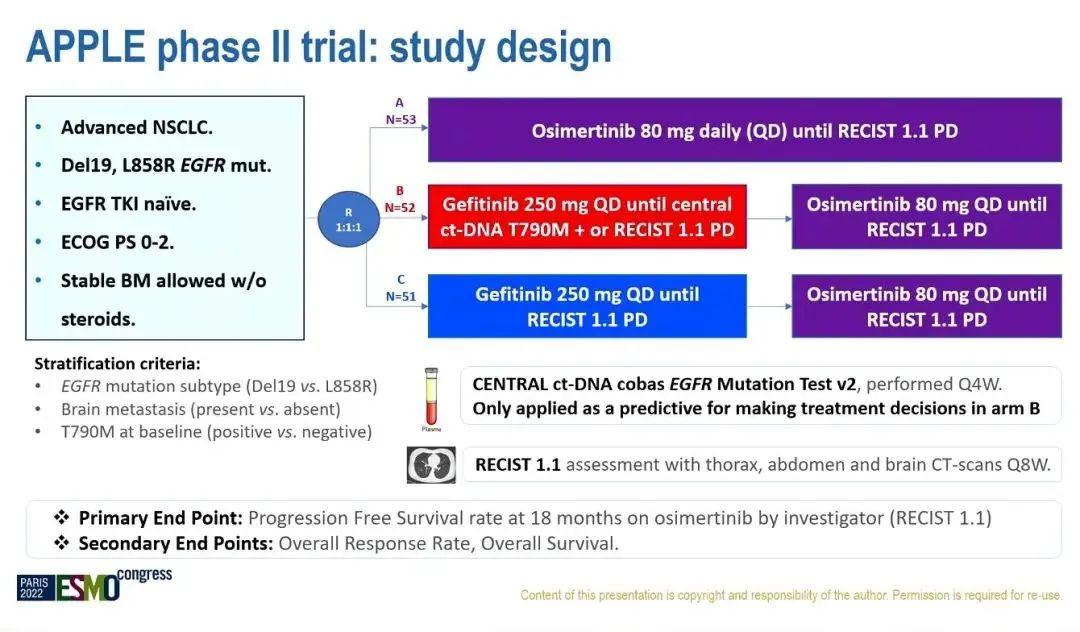
APPLE研究是一项在EGFR突变初治NSCLC患者中开展的随机、非比较、开放标签、3臂的Ⅱ期研究,旨在评估血浆EGFR T790M监测的可行性,以及从吉非替尼转换至奥希替尼的最佳节点探索。
图. APPLE研究设计
2022年ESMO大会上公布了B组(吉非替尼治疗至使用ct-NDA cobas EGFR test v2显示EGFR T790M突变+或按照RECIST 1.1标准评估出现疾病进展)和 C组(吉非替尼治疗至按照RECIST 1.1标准评估出现疾病进展),进展后转换至奥希替尼治疗的结果。结果显示,通过ctDNA连续监测T790M状态,可在疾病进展前(按RECIST标准评估)识别出17%的分子学进展患者,并指导更早地转换奥希替尼治疗。B组和C组在使用奥希替尼治疗18个月时的无进展生存(PFS)率方面分别为67.2%和53.5%,中位总生存期(OS)分别为尚未达到和42.8个月,18个月OS率分别为87%和77%。期待本次大会上该研究A组数据和OS相关结果的公布。 2O - Phase II Randomized Study of Osimertinib (OSI) With or Without Local Consolidative Therapy (LCT) for Metastatic EGFR Mutant Non-Small Cell Lung Cancer (NSCLC): Analysis of Adverse Events (AEs)
奥希替尼±局部巩固治疗(LCT)EGFR突变转移性NSCLC的Ⅱ期随机研究的不良事件(AE)分析
目前越来越多的证据表明,在奥希替尼治疗后合并寡转移的EGFR突变转移性NSCLC 患者中应用LCT,如外科手术、放疗或放疗+手术,可以改善患者的PFS和OS。奥希替尼+LCT的AE与奥希替尼单药治疗相比,是否发生率更高?强调疗效的同时,我们也关注安全性,本次大会将向我们揭晓相关的AE详情,从而更好的指导临床用药。
3O - Long-term efficacy, safety, and predictors of response to amivantamab among patients with post-platinum EGFR Ex20ins-mutated advanced NSCLC
Amivantamab治疗含铂化疗经治的EGFR 20外显子插入突变(ins)晚期NSCLC的长期疗效、安全性和疗效预测标志物
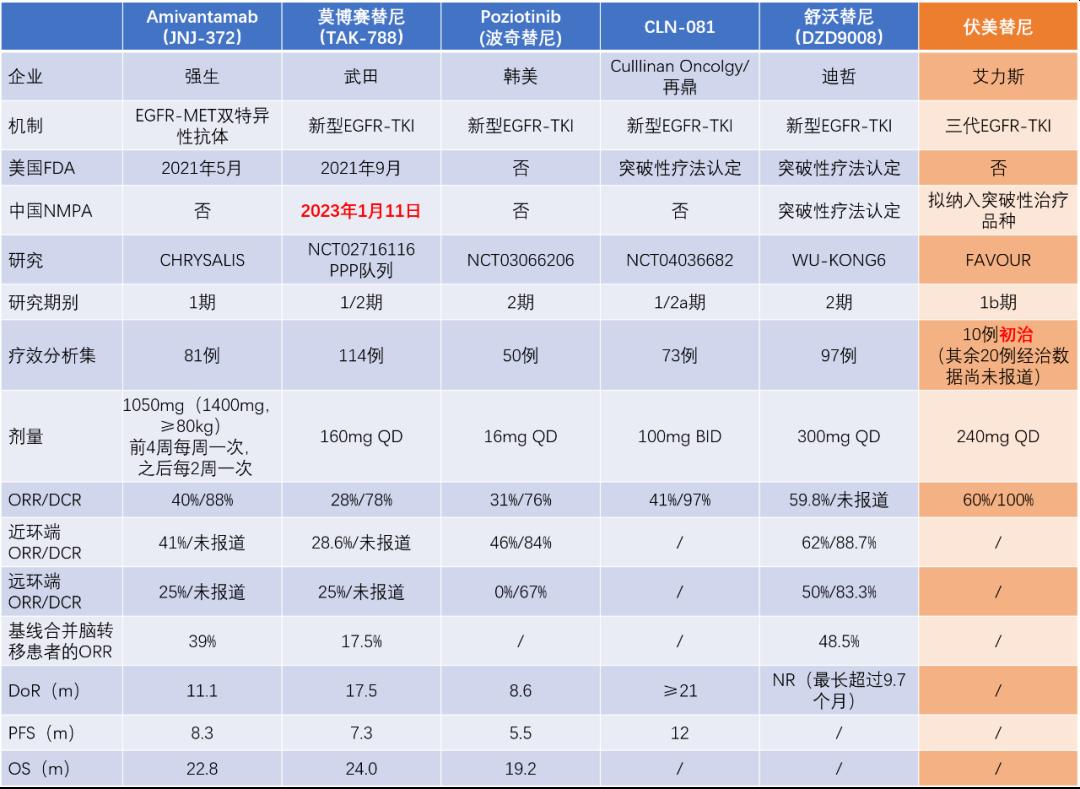
EGFR 20ins对传统EGFR-TKI不敏感,对化疗和免疫治疗的疗效也不尽如人意,这类患者的预后较EGFR敏感突变患者更差。近年来一些新药探索了含铂化疗经治的EGFR 20ins突变晚期NSCLC的治疗。2021年5月,EGFR-MET双特异性抗体Amivantamab(JNJ-372)凭借Ⅰ期CHRYSALIS研究结果率先获得美国FDA批准,打破EGFR 20ins突变无药可用的窘境,具有里程碑式的意义。该研究结果显示,总人群的客观缓解率(ORR)为40%,中位PFS为8.3个月,中位OS为22.8个月,该终点仍不成熟。期待本次大会报道其长期疗效、安全性和疗效预测标志物等临床关注的数据。
表. EGFR 20ins领域重要研究及数据汇总
(蓝色:含铂化疗经治;橙色:初治)
相关阅读
1. 一表汇总EGFR 20ins领域值得关注的研究结果,舒沃替尼≥2线治疗ORR 59.8%创新高!
4O - Patient-reported outcomes from the CodeBreaK 200 phase 3 trial comparing sotorasib versus docetaxel in KRAS G12C-mutated NSCLC
3期CodeBreaK 200研究索托雷塞 vs 多西他赛治疗经治KRAS G12C突变NSCLC的患者报告结局
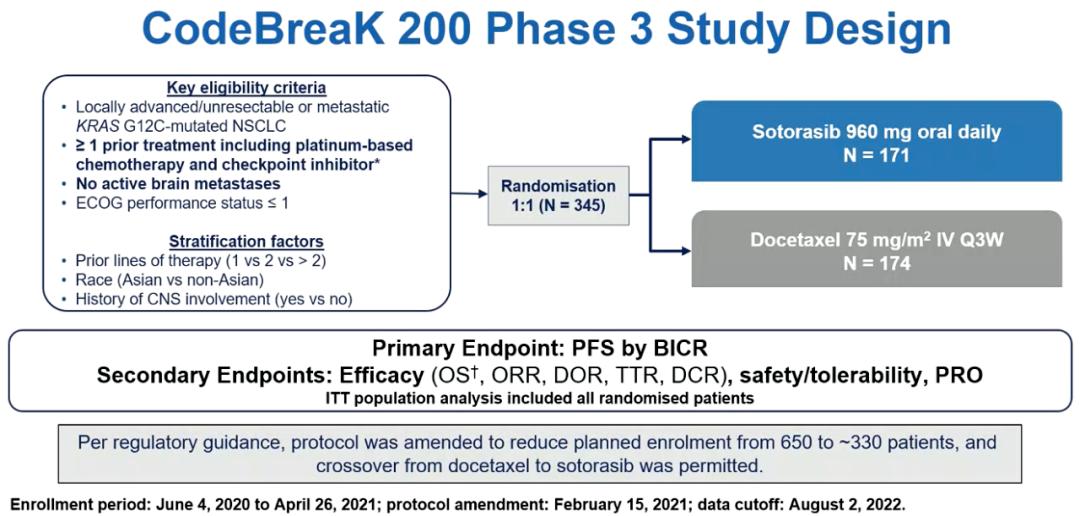
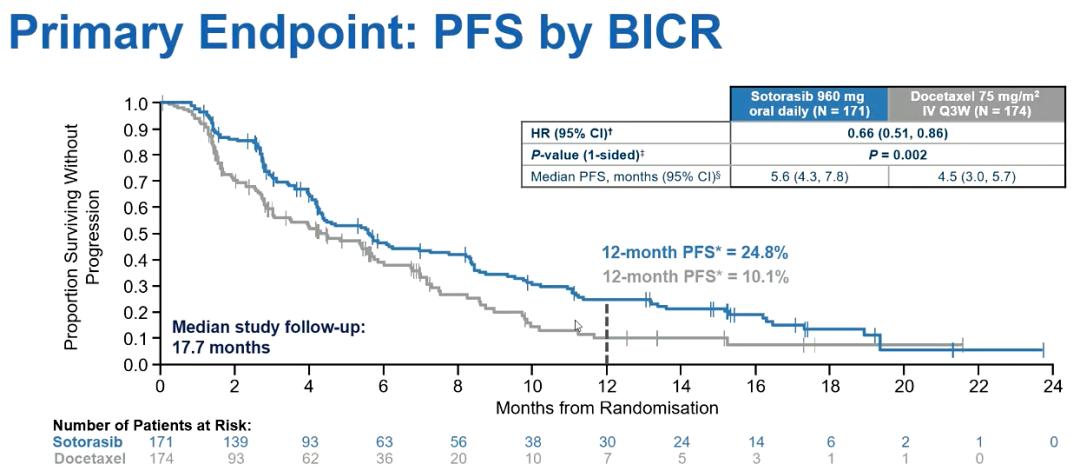
KRAS突变在NSCLC中的发生率约20%~30%,其中G12C突变最为常见,约占13%。基于1/2期CodeBreaK 100研究结果,2021年5月,索托雷塞获得美国FDA批准,成为首个针对KRAS突变的靶向药物,2021年9月,索托雷塞顺利落地我国海南博鳌乐城医疗先行区,中国患者也可合法使用。2022年ESMO大会上报道了CodeBreaK 200研究结果,索托雷塞 vs 多西他赛的中位PFS为5.6个月 vs 4.5个月(HR=0.66,P=0.002),ORR为28.1% vs 13.2%(P<0.001),中位OS没有显著差异,为10.6个月 vs 11.3个月(HR=1.01,P=0.53)。本次大会将报道CodeBreaK 200研究的患者报告结局。
图. CodeBreaK 200研究设计
图. CodeBreaK 200研究主要终点PFS 相关阅读
84O - Neoadjuvant nivolumab (N) + platinum-doublet chemotherapy (C) for resectable NSCLC: 3-y update from CheckMate 816
CheckMate 816研究3年数据更新:纳武利尤单抗+含铂双药化疗新辅助治疗可切除NSCLC
既往数据显示,在可切除NSCLC患者中,纳武利尤单抗+含铂双药化疗 vs 单纯化疗新辅助治疗,
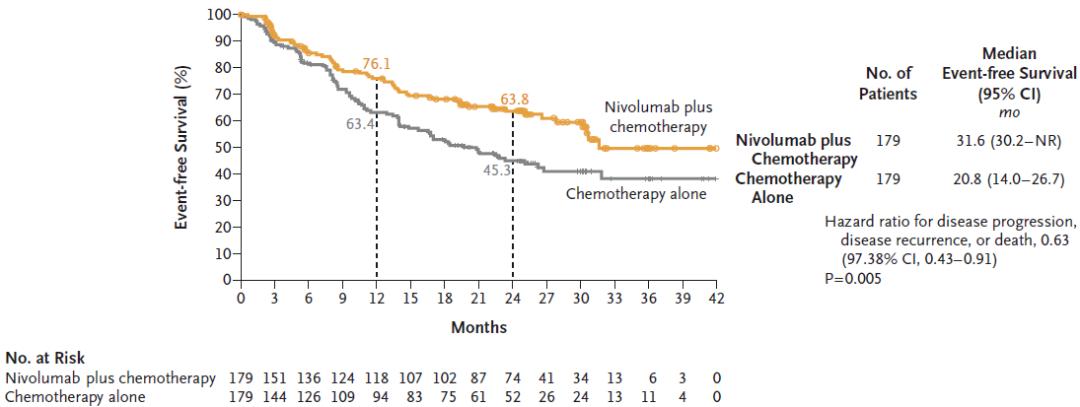
中位EFS:31.6个月 vs 20.8个月(HR=0.63,P=0.005);
2年EFS率:63.8% vs 45.3%;
pCR率:24.0% vs 2.2%(OR=13.94,P<0.001);
OS:具有获益趋势(HR=0.57,P=0.0079);
2年OS率:82.7% vs 70.6%;
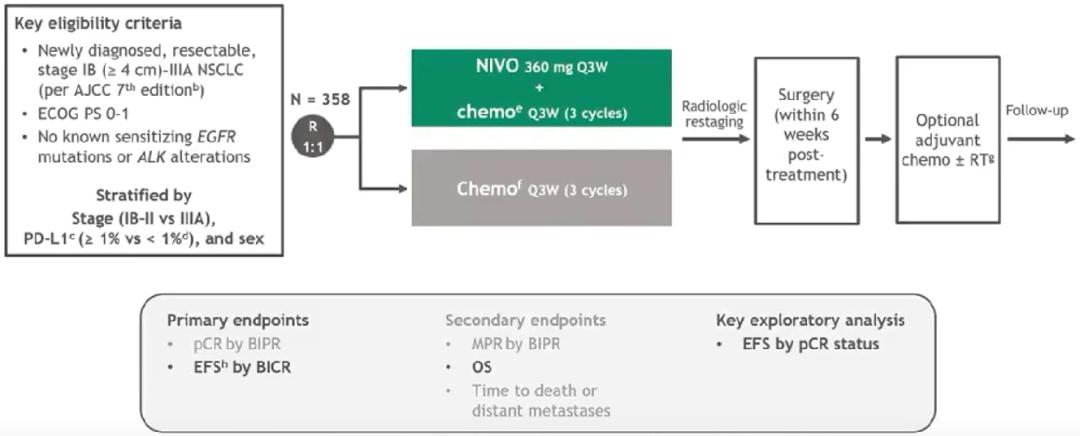
基于该研究结果,2023年1月,NMPA批准纳武利尤单抗新增适应证,联合含铂双药化疗(每3周一个周期,持续3个周期),用于可切除的(肿瘤≥4cm或淋巴结阳性)NSCLC成人患者的新辅助治疗,无论PD-L1表达水平。纳武利尤单抗成为中国首个且目前唯一获批用于NSCLC新辅助治疗的免疫检查点抑制剂。本次大会将报道3年随访的更新数据,两组在3年EFS率、3年OS率上会拉开怎样的差距?让我们拭目以待。
图. CheckMate 816研究设计
图. CheckMate 816研究共同主要终点EFS
相关阅读
1. 开创先河!O药获批中国首个且目前唯一NSCLC新辅助治疗适应证
2. CheckMate 816研究AACR&NEJM同步发表!纳武利尤单抗+化疗新辅助治疗显著延长EFS近1年,达31.6个月
5O - Cemiplimab plus chemotherapy versus chemotherapy alone in non-small cell lung cancer: longer follow-up results from the Phase 3 EMPOWER-Lung 3 trial
3期EMPOWER-LUNG 3研究长期随访结果:Cemiplimab +化疗 vs 单纯化疗一线治疗晚期NSCLC
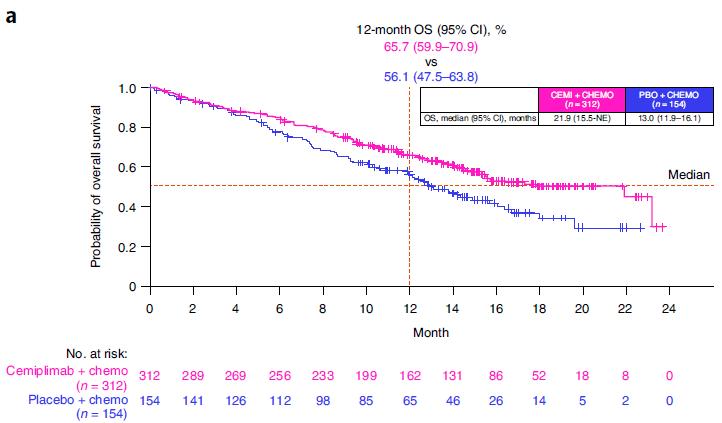
既往数据显示,对于驱动基因阴性晚期NSCLC,PD-1抑制剂Cemiplimab+化疗组 vs 单纯化疗组一线治疗的中位OS为21.9个月 vs 13.0个月(HR=0.71),中位PFS为8.2个月 vs 5.0个月(HR=0.56),ORR分别为43%和23%。基于此,2022年11月,美国FDA批准抗Cemiplimab+铂类化疗用于无EGFR突变、ALK融合或ROS1 突变的晚期NSCLC成人患者的一线治疗。本次大会将告诉我们,Cemiplimab是否如其他PD-1/L1药物一样具有免疫长拖尾效应,给患者带来长期的临床获益?
图. EMPOWER-LUNG 3研究OS(a)和PFS(c)
6O - CONTACT-01: Efficacy and safety from a Ph 3 study of atezolizumab (atezo) + cabozantinib (cabo) vs docetaxel (doc) monotherapy in patients (pts) with metastatic NSCLC (mNSCLC) previously treated with checkpoint inhibitors and chemotherapy
3期CONTACT-01研究:阿替利珠单抗+卡博替尼 vs 多西他赛单药治疗既往免疫检查点抑制剂和化疗经治的转移性NSCLC的疗效和安全性
2022年12月,益普生(Ipsen)宣布,其多靶点TKI卡博替尼的Ⅲ期CONTACT-01研究未达到显著延长OS的主要终点,但未公布具体数据。该研究共纳入366例患者,旨在评估卡博替尼+阿替利珠单抗 vs 多西他赛治疗既往免疫检查点抑制剂和含铂化疗经治、驱动基因阴性的转移性NSCLC的疗效和安全性。主要研究终点是OS,次要终点包括PFS、ORR和缓解持续时间。本次大会将报道该阴性研究的详细数据,有助于我们分析和反思其失败原因。
161O - RESILIENT Part 2: A Randomized, Open-label Phase 3 Study of Liposomal Irinotecan versus Topotecan in Adults with Relapsed Small Cell Lung Cancer (SCLC)
RESILIENT研究第2部分:伊立替康脂质体 vs 拓扑替康治疗复发性小细胞肺癌(SCLC)的随机、开放标签、3期研究
RESILIENT研究第2部分纳入一线含铂化疗或放化疗(包括用于局限期或广泛期SCLC治疗)期间或之后疾病进展的SCLC患者,比较伊立替康脂质体 vs 拓扑替康的疗效。第2部分的主要终点为OS,次要终点包括ORR、PFS、生活质量和安全性。与拓扑替康相比,伊立替康脂质体作为二线治疗的OS没有优势,未达到第2部分的主要终点。尽管如此,试验组患者的ORR比拓扑替康组患者提高了1倍。根据此前Ⅱ/Ⅲ期临床试验结果,美国FDA于2020年12月批准伊立替康脂体作为SCLC患者的二线治疗药物。本次分析将有助于我们深入了解SCLC的复杂性,以及伊立替康脂质体在SCLC领域的下一步计划。 参考文献
REFERENCES
https://www.esmo.org/meeting-calendar/european-lung-cancer-congress-2023
编辑|梅婕
审核|叶静 责编|赵德云
— END — CCMTV肿瘤频道视频号已上线!
带您洞察肿瘤前沿资讯 精彩不断,敬请关注!
点击下方“阅读原文” 访问更多CCMTV肿瘤科频道精彩内容
二维码
关注CCMTV

CCMTV APP下载

关注CCMTV云管家